Comment savoir que l’eau est à 100 ?

Comment savoir si l’eau est à 100 degrés ? Gardez votre main près de l’eau. Si vous voulez savoir si l’eau est froide, chaude ou tiède, placez d’abord votre main dessus. Ceci pourrez vous intéresser : Comment toucher un héritage ?. Si vous sentez la chaleur s’évaporer de l’eau, c’est qu’elle est chaude et que vous risquez de vous brûler.
Comment connaître la température de l’eau ? Pour évaluer la température d’une eau, il suffit d’écouter attentivement : dès 80°C les premières rumeurs se font entendre. L’eau commence à se fissurer puis une note continue se forme autour de 82°C. à 87°C une deuxième note apparaît et le volume augmente au fur et à mesure que le degré progresse.
Comment savoir que l’eau est à 90 degrés ?
Pour détecter une eau chaude à 80°C, il suffit d’écouter. C’est à ce moment que l’eau commence à faire du bruit dans le récipient. Lire aussi : Où trouver des médicaments le dimanche ?. Si ces bruits sont continus et atténués, vous devez être entre 82 et 90°C. Puis soudain plus de bruit.
Comment connaître température eau sans thermomètre ?
4 – Connaître la température de l’eau sans thermomètre Si vous avez de très petites bulles dans votre eau chaude, de la taille d’une tête d’épingle, alors elle est à environ 71°C. Dès que l’eau chaude atteint 79 ° C, vous pouvez vaporiser du fond de l’eau chaude jusqu’à des bulles plus grosses.
Comment obtenir une eau à 90 ?
# 2 : Système D : Mélanger de l’eau chaude et de l’eau froide Par exemple, si vous souhaitez préparer un thé vert à 70°, comptez deux tiers de l’eau bouillante pour un tiers de l’eau froide. Pour un thé à 80°, ils n’ajoutent qu’un quart d’eau froide, et pour un thé à 90° qu’un dixième.
Comment savoir si l’eau est à ébullition ?
Cuisson : il y a de la vapeur et un mouvement perpétuel qui ne s’arrête pas lorsque vous remuez l’eau. C’est le palier le plus chaud que votre eau puisse atteindre : 100°C. A voir aussi : Comment se procurer un plan de bornage ?. A cette température, vous pouvez cuire des pâtes.
Comment savoir que l’eau bout ?
Ainsi, déterminer son point d’ébullition n’est pas aussi simple qu’il y paraît. « L’eau bout à 100°C à la pression atmosphérique normale », a-t-on appris.
Comment porter à ébullition de l’eau ?
Si vous souhaitez faire bouillir l’eau plus rapidement, il faut programmer et/ou remuer à plus de 100° (en partie basse).
Comment mesurer la température de l’eau sans thermomètre ?
4 – Connaître la température de l’eau sans thermomètre Si vous avez de très petites bulles dans votre eau chaude, de la taille d’une tête d’épingle, alors elle est à environ 71°C. Dès que l’eau chaude atteint 79 ° C, vous pouvez vaporiser du fond de l’eau chaude jusqu’à des bulles plus grosses.
Comment savoir si l’eau est à 60 degrés ?
Plongez votre coude dans l’eau. Si le réservoir d’eau est assez grand, trempez un de vos coudes dans l’eau. Cela vous donne une idée de sa température. Vous pouvez dire tout de suite s’il fait chaud ou froid.
Comment savoir si l’eau est à 70 ?
De l’eau à 70°C En chauffant l’eau, une des premières réactions observées est la formation de petites bulles. On estime que lorsque les premières petites bulles (de la taille d’une tête d’épingle) commencent à se former sur le fond du récipient, l’eau est alors aux alentours de 70°C.
Quels sont les noms des changements d’état exothermique expliquez pourquoi ?
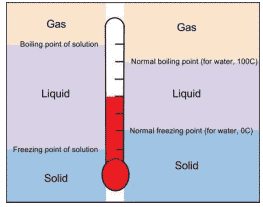
La fusion, l’évaporation et la sublimation sont des changements d’état endothermiques. En revanche, la solidification, la liquidité et la condensation sont des changements d’état exothermiques.
Pourquoi la solidification est-elle exothermique ? Lorsque l’eau H2O passe de l’état liquide à l’état solide, on parle de processus de solidification. Sur le plan énergétique, ce processus libère de l’énergie dans l’environnement (le processus est dit exothermique), c’est-à-dire les molécules d’eau perdent de la chaleur lorsqu’elles sont à l’état solide.
Quels sont les 6 changements d’état possible ?
2) Changements d’état de fusion : passage de l’état solide à l’état liquide. Évaporation : passage de l’état liquide à l’état gazeux. Liquéfaction : Passage d’un état gazeux à un état liquide. Solidification : Passage de l’état liquide à l’état solide.
Comment Appelle-t-on les différents changements d’état ?
Changements d’état de la matière Lorsqu’un liquide devient gaz, on parle d’évaporation ; Lorsqu’un gaz devient liquide, on l’appelle liquide ; Lorsqu’un gaz se solidifie, on parle de condensation ; Lorsqu’un solide devient un gaz, on parle de sublimation.
Quels sont les 4 changement d’état de l’eau ?
Modifications de l’état de l’eau A la pression atmosphérique normale (1013,25 hPa) c’est de l’eau pure, distillée solide (glace) pour les températures inférieures à 0°C, liquide pour une température comprise entre 0°C et 100°C, et à l’état gazeux. (Vapeur d’eau) pour des températures plus élevées.
Quel est le nom du premier changement d’état de l’or ?
Solidification Il est donc nécessaire d’abaisser la température pour transformer une substance à l’état liquide initialement à l’état solide. Pour fabriquer des lingots d’or, l’or est fondu et une forme liquide est versée dans le moule. Lorsque l’or est renforcé, le moule est retiré.
Comment Appelle-t-on le passage de l’état liquide à l’état gazeux ?
La transition inverse (de l’état liquide à l’état solide) est appelée solidification. … Le passage de l’état liquide à l’état gazeux est appelé évaporation, tandis que la régression (de l’état gazeux à l’état liquide) est appelée liquide.
Quel est le nom de changement de phase qui permet d’abaisser la température corporelle lors de la sudation ?
La thermorégulation est sous le contrôle de l’hypothalamus et a pour fonction de contrôler la température corporelle. En s’élevant, l’hypothalamus met en place différents processus pour évacuer l’excès de chaleur et maintenir une température corporelle plus ou moins constante.
Comment Appelle-t-on les différents changements d’état ?
Changements d’état de la matière Lorsqu’un liquide devient gaz, on parle d’évaporation ; Lorsqu’un gaz devient liquide, on l’appelle liquide ; Lorsqu’un gaz se solidifie, on parle de condensation ; Lorsqu’un solide devient un gaz, on parle de sublimation.
Comment s’appelle le changement d’état de l’eau ?
Le passage de l’état liquide à l’état solide est appelé solidification. Inversement, lorsque de l’eau solide (par exemple de la glace) fond et devient liquide, on parle de fusion. 2/ De l’état liquide à l’état gazeux : Le passage de l’état liquide à l’état gazeux est appelé évaporation.
Quels sont les 4 changement d’état de l’eau ?
Modifications de l’état de l’eau A la pression atmosphérique normale (1013,25 hPa) c’est de l’eau pure, distillée solide (glace) pour les températures inférieures à 0°C, liquide pour une température comprise entre 0°C et 100°C, et à l’état gazeux. (Vapeur d’eau) pour des températures plus élevées.
Comment savoir si c’est un corp pur ou un mélange ?

Une substance pure est une substance composée d’une seule espèce chimique. Un mélange se compose d’au moins deux types. On distingue les mélanges homogènes pour lesquels une seule phase est distinguée et les mélanges hétérogènes pour les différentes phases.
Comment savoir si une solution est un corps pur ou un mélange ? Différence entre corps pur et mélange. Une substance pure est un matériau d’un seul type chimique, par opposition à un mélange qui en contient plusieurs. Une substance pure simple est constituée d’une seule espèce atomique (Exemple : Fer, Fe ; Dioxygène, O2(g) â € ¦).
Comment savoir si un corp est pur ?
Une substance, qu’elle soit solide, liquide ou gazeuse, est qualifiée de « substance pure » si, contrairement à un mélange, elle n’est constituée que d’une espèce chimique.
Quelles sont les caractéristiques d’un corps pur ?
Propriétés des corps purs Ce sont principalement leurs points de fusion et d’ébullition, leur indice de réfraction, leur densité, leurs conductivités électriques et thermiques, etc. Un échantillon d’une substance pure aura des propriétés identiques à celles de l’ensemble.
Comment reconnaître si un corps est pur ?
Définition d’un corps pur : Un corps pur est une substance d’une seule espèce chimique. Définition d’un mélange : Un mélange est une substance de différents types chimiques. Définition d’un mélange homogène : Un mélange est homogène si aucun composant ne peut être distingué à l’œil nu.
Est-ce que tout les corps se solidifie à 0 C ?

Le renforcement d’un corps pur dans un mélange. A noter que la courbe de renforcement de l’eau pure forme un plateau à 0°C. … Pour tous les corps purs, il existe de la même manière un plateau au changement d’état et la température à laquelle ce plateau se produit est caractéristique d’un certain corps pur.
Quel est l’état physique de l’eau salée à 0 C ? Mais l’eau salée a une température de fusion plus basse que l’eau pure et gèle en dessous de 0°C. Le mélange eau/sel ne peut pas se solidifier car la température du mélange monte alors pour s’adapter au milieu (-2°C par exemple) et reste liquide car il n’est qu’à -21° vs.
Comment savoir si c’est un corps pur sur un graphique ?
Vous devez analyser le graphique tracé pour identifier le corps. On réalise la fusion d’un corps. La température corporelle est prise toutes les minutes pendant 10 minutes. Sur la base de ces valeurs et à l’aide de données de température sur les changements d’état de différents corps, identifiez le corps à l’étude.
Comment savoir si un corps est pur ?
Une substance, qu’elle soit solide, liquide ou gazeuse, est qualifiée de « substance pure » si, contrairement à un mélange, elle n’est constituée que d’une espèce chimique.
Comment savoir si un solide est un corps pur ?
Un corps pur est une substance (solide, liquide ou gazeuse) constituée d’un seul type de molécule. Exemples : L’eau distillée est une substance pure car elle est constituée uniquement de molécules d’eau. Le dioxygène est une substance pure car il est constitué uniquement de molécules de dioxine.
Quels sont les 4 changement d’état ?
Lorsque la matière passe d’un état à un autre état, on dit que c’est un changement d’état.
- Transition solide-liquide : fusion. …
- Transition liquide-solide : Renforcement. …
- Transition gaz liquide : évaporation. …
- Transition solide-gaz : sublimation. …
- Transition gaz-solide : Condensation. …
- Transition gaz-liquide : Liquide.
Comment s’appelle le passage d’un état à un autre ?
Le passage d’un état à un autre a des noms : Condensation : C’est le passage d’une forme gazeuse à un état liquide. Il y a aussi la condensation solide, qui est le passage de l’état gazeux au solide sans passer par la phase liquide. L’évaporation : c’est le passage de l’état liquide à l’état gazeux.
Quels sont les 4 changement d’état de l’eau ?
Modifications de l’état de l’eau A la pression atmosphérique normale (1013,25 hPa) c’est de l’eau pure, distillée solide (glace) pour les températures inférieures à 0°C, liquide pour une température comprise entre 0°C et 100°C, et à l’état gazeux. (Vapeur d’eau) pour des températures plus élevées.
Est-ce que l’alcool est un corps pur ?
En tant que substance pure (100% d’alcool), l’éthanol ne contient que des molécules d’éthanol. Le point d’ébullition de l’éthanol est de 78°C dans des conditions normales de pression : c’est une caractéristique physique de l’éthanol.
Est-ce que tous les corps purs sont homogènes ?
b â € « Toutes les substances homogènes sont des corps purs. Faux, il existe des mélanges homogènes comme le sirop de menthe.
Quels sont les corps purs ?
Il existe deux types de corps purs : les corps purs simples et les corps purs composés. Une substance pure simple se compose d’un seul type d’atomes. Exemple : Argent Ag, Carbone C, Dioxygène O 2. Un corps pur composé est un corps pur composé de différents types d’atomes.
Pourquoi l’eau bout à 100 degrés ?
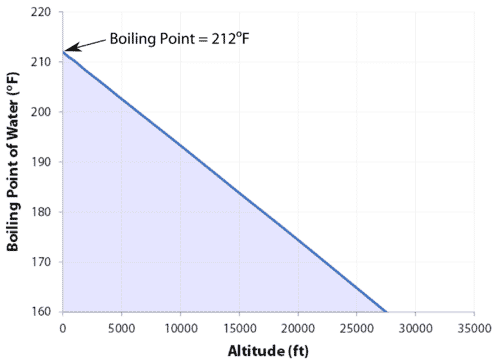
La pression exercée sur l’eau lorsque le récipient est ouvert est la pression atmosphérique. A 1013 hPa, l’eau bout à 100°C. Lorsque la pression sur l’eau est inférieure à la pression atmosphérique, l’eau bout à une température inférieure à 100°C.
L’eau bout-elle toujours à 100°C ? « L’eau bout à 100°C à la pression atmosphérique normale », nous a-t-on dit. … Et les niveaux de température ne sont devenus internationaux Celsius qu’en 1948.
Pourquoi l’eau ne dépasse pas les 100 degrés ?
Ainsi, même si la température descend en dessous de 0°C, l’eau passe directement de l’état solide à l’état liquide. C’est ce qu’on appelle la sublimation. En résumé, l’eau ne gèle qu’à 0°C et bout à 100°C sous pression atmosphérique normale.
Pourquoi l’eau bout A moins de 100 C ?
A 1013 hPa, l’eau bout à 100°C. Lorsque la pression sur l’eau est inférieure à la pression atmosphérique, l’eau bout à une température inférieure à 100°C.
Pourquoi l’eau s’évapore A moins de 100 C ?
A température ambiante, il se produit une certaine agitation (thermique) des molécules d’eau, qui provoque l’éjection de certaines d’entre elles hors du liquide. Une fois éjectées, les molécules peuvent être renvoyées dans le liquide ou s’en éloigner, selon les chocs qu’elles subissent avec les molécules d’air.
Pourquoi l’eau Bout-elle à 100 ?
Ainsi sous 1 atmosphère, qui est la pression atmosphérique normale, l’eau bout en fait à 100°C. Au fur et à mesure que la pression monte, on voit que la température de cuisson monte également : il faudra chauffer davantage pour obtenir de la vapeur. C’est le cas au fond des océans, où la pression augmente fortement.
Est-ce que l’eau bouille toujours à 100 C ?
« L’eau bout à 100°C à pression atmosphérique normale », a-t-on appris. … C’est ainsi que le Suédois Anders Celsius définissait son échelle de température au début du 18e siècle. De plus, au début, le 0 de son échelle marquait le point d’ébullition et le 100 le point de congélation.
Pourquoi la température d’ébullition de l’eau est si élevée ?
L’eau absorbe de l’énergie sous forme de chaleur, ce qui élève la température de l’eau jusqu’à 100°C. Lorsque l’eau commence à bouillir, l’énergie absorbée permet le changement d’état à température constante.
Quelle est la température de solidification et de fusion de l’eau pure ?
L’eau est une substance pure qui se conserve à une température constante de 0°C (mesurée sous la pression atmosphérique normale au niveau de la mer). La température de fusion de la glace est également égale à 0°C. Pour un mélange (cas de l’eau sucrée) la température de solidification varie.
Comment la température de fusion et d’amplification de l’eau pure se compare-t-elle ? On dit que le point de fusion de l’eau est de 0°C. Lorsque la glace et l’eau liquide coexistent, la température est de 0°C : La fonte et le renforcement de l’eau s’effectuent à une température constante.
Quelle est la température de la fusion ?
| Corps pur | Température de fusion (°C) | Cuisson / Température liquide (°C) |
|---|---|---|
| L’eau | 0°C | 100°C |
| Cyclohexane | 6°C | 81°C |
| Merkur | 39°C | 357°C |
| Fer | 1535°C | 2750°C |
Quelle est la température de fusion de l’eau ?
L’eau est une substance pure qui se conserve à une température constante de 0°C (mesurée sous la pression atmosphérique normale au niveau de la mer). La température de fusion de la glace est également égale à 0°C.
Quelle est la température de l’ébullition ?
Ainsi, déterminer son point d’ébullition n’est pas aussi simple qu’il y paraît. « L’eau bout à 100°C à la pression atmosphérique normale », nous a-t-on dit.
Quelle est la température de solidification de leau pure ?
Un simple refroidissement peut suffire à renforcer un liquide. Ainsi, la température de solidification de l’eau pure sous pression atmosphérique est de 0°C.
Quel est la température de solidification de l’eau ?
– La notion essentielle (renforcement à 0°C) semble être captée pour 23 des 24 élèves de CE2. – Le changement d’état à température constante n’est détecté que par 5 des 24 élèves. Pour d’autres, la température baisse et varie en conséquence. La phase de changement d’état est considérée comme l’ensemble de l’expérience.
Quel est la température de l’eau pure ?
« L’eau bout à 100°C à la pression atmosphérique normale », nous a-t-on dit. Pourquoi l’eau bout à 100° et gèle à 0° ? Car c’est ainsi que le Suédois Anders Celsius définissait son échelle de température au début du 18ème siècle.
Quelle différence y A-t-il entre la solidification de l’eau pure et la solidification de l’eau salée ?
A noter que la courbe de destruction de l’eau pure forme un plateau à 0°C. C’est à cette température que se produit le changement d’état de l’eau liquide en eau solide. … L’eau salée n’est pas un corps pur. Pour un mélange d’eau et de sel il n’y a pas de niveau car c’est un mélange.
Quel est la température de solidification de l’eau ?
– La notion essentielle (renforcement à 0°C) semble être captée pour 23 des 24 élèves de CE2. – Le changement d’état à température constante n’est détecté que par 5 des 24 élèves. Pour d’autres, la température baisse et varie en conséquence. La phase de changement d’état est considérée comme l’ensemble de l’expérience.
Quels sont les 4 changement d’état de l’eau ?
Modifications de l’état de l’eau A la pression atmosphérique normale (1013,25 hPa) c’est de l’eau pure, distillée solide (glace) pour les températures inférieures à 0°C, liquide pour une température comprise entre 0°C et 100°C, et à l’état gazeux. (Vapeur d’eau) pour des températures plus élevées.
Sources :




